临床CRO
三个皮匠报告为您整理了关于临床CRO的更多内容分享,帮助您更详细的了解临床CRO,内容包括临床CRO方面的资讯,以及临床CRO方面的互联网报告、券商研究报告、国际英文报告、公司年报、招股说明书、行业精选报告、白皮书等。
1、 公司编制谨请参阅尾页的重要声明 家用器械家用器械领军企业领军企业,临床,临床协同协同迎风起航迎风起航 证券证券研究报告研究报告 所属所属部门部门 行业公司部 报告报告类别类别 公司深度 所属行业所属行业 医药生物 报告报告时间时间 2020/1/22 前收盘价前收盘价 22.20 元 公司评级公司评级 增持评级 分析师分析师 周豫周豫 证书编号:S1100518090001。
2、CRO&CDMO投研体系之数据跟踪(系列二)投研体系之数据跟踪(系列二): 国内国内CRO&CDMO行业,核心数据回顾与行业,核心数据回顾与2020年前瞻年前瞻 行业投资建议: 领先大市-A 安信证券研究中心安信证券研究中心 首席分析师:马首席分析师:马 帅帅 S1450518120001 联联分分系系分分人:冯雪云人:冯雪云 S1450119080031 2020年年02月月 。
3、CRO&CDMO投研体系之行业深度报告(系列一)投研体系之行业深度报告(系列一) 安信证券研究中心安信证券研究中心 首席分析师:马首席分析师:马 帅帅 S1450518120001 联联分分系系分分人:冯雪云人:冯雪云 S1450119080031 2020年年01月月 行业投资建议: 领先大市-A 国内国内CRO&CDMO行业:高景气背景下的追赶与跨越行业:高景气背景下的追赶与跨。
4、请务必阅读正文之后的免责条款部分请务必阅读正文之后的免责条款部分 2020.01.12 创新浪潮助推创新浪潮助推 CRO/CDMO 行业加速蜕变行业加速蜕变 丁丹丁丹(分析师分析师) 张祝源张祝源(分析师分析师) 0755-23976735 021-38674623 Z 证书编号 S0880514030001 S0880519090001 本报告导读:本报告导读: 新药研发高景气度。
5、评价获得的,凝聚着专家共识的知识不仅仅是机器学习内容的重要来源,其知识本身所包含的诊疗逻辑也是指导机器作出可解释行为的重要依据。 但人与机器有着各自的语言体系,因此知识表达形式的转换是必经之路。 内容摘要计算机化临床实践指南的定义、应用方向和价值临床实践指南是临床决策中不可缺少的部分,它能够指导医疗服务者更好地进行诊断治疗。 然而目前临床实践指南基本以文本格式发布,不利于医护人员实际工作中的使用。 因此让计算机去理解指南的内容和逻辑关系,并将这些逻辑关系整合到用于健康医疗环境中的信息系统中,即临床指南计算机化,成为了一个重要的研究方向。 当前计算机化临床指南主要用于为临床辅助决策系统提供基础支撑。 具体应用模式上,计算机化临床指南一般与电子病历数据及信息系统相结合,使决策支持系统能够结合患者信息执行指南,在诊疗环节提供针对性建议,指导临床实践、规范诊疗流程,减轻医护人员的工作强度,提高医疗质量。 临床指南计算机化的技术实现方式临床指南计算机化一般可以分为建模和执行两个层面。 建模层面,目前大多数的建模方法都来自于国外的一些科研项目,大致可以分为基于文档的建模和基于知识的建模两种。 基于文档的建模属于文档层面的结构化,侧重于将指南文档表示为机器可读的形式,来促进指南的应用;基于知识的建模则侧重于将指南中的知识表示为机器可理解的形式,作为构建临床辅助决策系统中知识。
6、洲特有的基因组数据,并帮助推进精准医学的努力。 精准医学研究基因组学实现模型如下: 该模型将遗传咨询和电子病历的访问权限作为护理整合的变量。 鉴于该项目的重点是全基因组筛选,不同结果的解释也是一个重要的进入点,以保证临床相关和可用的基因测试。 精准医学目前对许多人来说仍然是无法进入的。 对美国三个州的公共卫生项目的研究表明,需要有针对性地扩大服务不足人群的参与,增加提供者教育,并在发现遗传风险时实施保障措施以提供医疗保健。 根据诊断结果,卫生系统的支付者(保险人)必须改变政策,以便制定报销战略,从而扩大基因服务的覆盖面。 文本由木子日青 原创发布于三个皮匠报告网站,未经授权禁止转载。 数据来源:世界经济论坛:精准医学护理准备原则资源指南:护理整合。 点击下载PDF报告。
7、研究和数字端点的创建提供了一个门户。 数字终点是由传感器、可穿戴设备和其他数字健康技术(如可摄入设备和可植入设备)产生的数据产生的。 例如,使用一种定制的腕带设备,可以监测患者的心率变化,或测量帕金森病患者的步态。 如果实施得当,数字端点有可能使临床试验中的每一个利益相关者受益,包括主办方、站点和患者。 数字健康技术允许在个人日常生活中收集数据,最大限度地减少对临床现场就诊的需要。 此外,数字端点可以使用传感器以一种新的方式捕捉现有的测量数据,例如,使用智能设备或手机应用程序来测量咳嗽,而不是依靠病人在日记中记录咳嗽发作。 这种超越诊所围墙的更频繁和持续的监测可以补充或取代传统的观察性评估,提供更精确和准确评估的可能性。 在这种情况下,一种设备用于改变临床环境中更常规的评估的给药模式;因此,传统上在临床中采集的血压现在可以在家庭环境中使用连接的数字血压监测器进行采集。 数字健康技术可以捕捉到一系列生理参数:文本由木子日青 原创发布于三个皮匠报告网站,未经授权禁止转载。 数据来源:ICON公司:通过临床开发管理可穿戴设备的数字端到端方法。
8、案。 利用数字健康作为干预措施在某些方面取得了成功,但患者获得新技术的机会可能有限,因此,在最有需要的地区采用创新的方法来预防艾滋病毒仍然是一个挑战。 智能手机技术的广泛采用导致了其作为提供针对PrEP的依从性干预措施的平台的流行。 目前临床试验的一个例子是P3(Prepared,Protected,emPowered),一款交互式智能手机应用程序,利用游戏机制和社交网络功能来提高PrEP依从性,16-24岁男男性接触者和男男性接触的年轻变性女性在PrEP临床护理中的保留率和PrEP持续性。 为艾滋病病毒携带者设计试验时应考虑以患者为中心艾滋病毒感染者面临歧视,这会对其生活质量和治疗结果产生负面影响。 因此,赞助者需要意识到与艾滋病毒有关的社会耻辱,包括参与艾滋病毒临床试验。 赞助商需要向员工和现场提供敏感性培训。 例如,考虑使用BYOD(自带设备)来减少耻辱感,而不是提供收集患者日记的智能手机,因为患者可能会被问及为什么以及如何收到新设备。 2021年及以后:艾滋病毒治疗的新前景2020年人们见证了从传统的抗逆转录病毒治疗组合(现有30多种抗逆转录病毒药物)到即将出现的新疗法的转变。 其中新研究产品包括广泛中和抗体(bNAbs)用于HIV预防和治疗,以及基于基因的治疗。 这些试验中最先进的是评估每八周静脉注射一次bNAb(称为VRC01)是否安全、可耐受和有效地预防HIV。 24种新型。
9、行业的临床还在20亿元,而临床前增加到了13亿元,药物发现也开始增到10亿元,且临床前的同比整速达到了30%。 2018年国内CRO行业在临床方面达到了30亿元,而临床前就有15亿元,药物发现有13亿元,且临床前的同比增速是15.4%;2019年国内CRO行业的规模是69亿元,其中临床有40亿元,临床前有18亿元,药物发现有11亿元,且临床前的同比增速为20.0%。 因此,我们预计2020年-2023年国内CRO行业最高规模达171亿元。 其中2020年CRO行业规模达80亿元、2021年行业规模达100亿元、2022年CRO行业规模达130亿元和2023年CRO行业规模达171亿元。 在预计2020年国内CRO行业规模中,临床行业规模40亿元左右,临床前行业规模20亿元,药物发现行业规模20亿元,其临床前同比增速是11.1%;预计在2021年临床行业规模达60亿元,临床前行业规模达24亿元,药物发现行业规模达16亿元,临床前同比增速20.0%;预计在2022年临床行业规模达到70亿元,临床前行业规模达29亿元,药物发现行业规模达31亿元;最后预计在2023年国内CRO行业中的临床行业规模达到了100亿元,临床前行业规模达35亿元,而药物发现行业规模达36亿元,且临床前行业规模同比增速是20.7%。 文本由栗栗-皆辛苦 原创发布于三个皮匠报告网站,未经授权禁止转载。 数据来源昭衍新药-国内。
10、们认为患者中心性在临床研究中表现为三个层次:1.策略层面:患者参与研究设计或与调控机构互动。 2.终点水平:患者在研究中完成了PROM或参与了PROM的开发和验证。 3.参与水平:患者与研究人员一起工作,以改善研究程序,促进研究中患者的招募和保留。 因此,我们利用这一视角来检查罕见病研究公开信息中明显的患者中心度。 具体来说,我们分析了从美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)网站上收集的关于PROMs在关键试验中使用的标签声明的数据和临床试验网站上的数据。 我们还对舞会行业的使用进行了广泛的文献综述。 病人参与在战略层面:罕见病患者宣传组织对于联系药物研究人员和临床试验潜在参与者的患者至关重要。 一般来说,赞助商会代表患者向PAOs寻求建议。 在欧洲罕见病对PAOs成员的调查中,超过一半的人在研究设计上建议研究人员一项罕见疾病临床研究网络(RDCRN)的研究发现,82%的主要研究人员报告称,患者审阅了研究方案,并“为研究设计提供了实质性的投入”。 然而,我们注意到,以这种方式涉及患者并非没有挑战。 患者很少接受这一角色的培训,他们通常必须克服财务和后勤障碍才能参加焦点小组。 赞助者还需要注意确保参与的患者确实是目标人群的代表。 文本由木子日青 原创发布于三个皮匠报告网站,未经授权禁止转载。 数据来源:ICON:罕见疾病患者药物开发结果衡量报告。
11、局(EMA)均于2013年发布了基于风险的监测指南,国际协调会议(ICH)指南Q9 中概述了质量风险管理原则。 FDA和EMA指南的目的是通过对研究行为和报告的最重要方面进行监督来提高临床试验中患者的安全性和数据质量。 一、ICON方法RBQM旨在预防,检测,减轻和学习临床试验中的风险和错误,同时保持符合法规指导的检查准备。 图1 RBOM框架在RBQM框架内,初始风险评估分类建议一种最佳的监测策略,而先发的临床试验风险则决定是否部署ICONIK集中式监测和分析。 ICONIK是功能强大的集成整合,标准化和可视化来自多个来源的运营和临床数据的信息平台,可提供所有研究信息的整体视图。 二、避免在可能的情况下,应考虑研究者和患者的观点,以便改进协议并在实现对研究过程的依从性方面最大程度地支持研究站点。 有效预防和获得高质量数据的下一步是有效的员工培训。 在RBQM框架内,FIRECREST培训解决方案提供定制的,基于研究的,基于Web的培训模块,以向现场人员和研究团队提供培训。 由研究人员领导的开发团队生成了动态且引人入胜的培训解决方案,以促进对现场人员和研究团队的培训。 三、探测RBQM通过将中央和现场监视整合到最佳技术,人员和过程范式中,从而能够设计出一种有效的检测方法,以实现质量,完整性,安全性以及性能风险和错误。 集中监控集中在集中的可视化数据或单个集合中的集中可用数。
12、 Healthcare Global Trends in Stem Cell Therapy Clinical Trials A 10-Year Retrospective, 20072016 Report Code: GDHC1299EI Published: June 2017 Global Trends in Stem Cell Therapy Clinical Trials 。
13、失败的临床试验可能会花费赞助商超过10亿美元,并且浪费数年时间开发一种永远无法上市的药物。 然而,这些损失现在可以通过使用人工智能(AI)和机器学习驱动的平台来减轻,这些平台可以在临床试验中确定对治疗有.。
14、p 项目管理和临床监测。 利用多年的经验站点数据库站点关系以及训练有素的员工优势,有效地开展和协调多站点IIIV期临床试验。 服务内容包括协议设计可行性运营计划站点启动患者招募和临床站点监视,通过将技术注入基于现场的监视来减少数据收集步骤和时。
15、3. 创新药大时代,国内CRO迎来大爆发pp3.1 国内CRO发展历程较短pp相较于海外CRO行业,国内CRO行业起步较晚,目前尚处于快速发展阶段。 pp上世纪90年代末期,以昆泰科文斯为代表的全球CRO巨头开始进军中国市场,形成了国内CR。
16、国内多家企业在本次 ASCO 大会上公布了旗下 PDL1 双抗的临床数据。 从与 PDL1 双抗搭档的靶点来看,CTLA4 的临床项目数量最多。 PDL1CTLA4 双抗有望凭借机制优 势改善伊匹木单抗在联用 PD1 单抗时毒性大治疗窗窄的限。
17、国内药品监管政策逐步与国际接轨。 2017 年6 月,原国家食品药品监督管理总局CFDA加入国际人用药品注册技术协调会ICH,正式成为 ICH 成员。 国家药监局将在 ICH 各项活动中发挥更加积极的作用,不仅可以参与 ICH 指导原则的制订。
18、员工规模持续扩张,员工总量行业领先。 IQVIA公司总人数从2013年28400人增至2020年70000人,复合增长率为13.8,2020年同比增长率为4.2020年,pp公司拥有临床医生和数据科学家共67000人,为100多个国家和。
19、公司是中国独立临床特检行业的领导者,也是血液学特检服务的主要供应商。 在过去17年中,已建立全面的检测组合广泛的医院网络及先进的技术平台,提供超过3,500种检验项目,在血液学遗传病及罕见病传染病肿瘤神经学及妇科相关疾病等各个专科领域,提供。
20、合成优化的高效性药物发现过程中,尤其是先导化合物发现后,一般会进行多轮合成优化寻找出合适的备选分子,以期药效药代动力学理化性质方面应达到一定要求。 这中间需要快速合成众多新型分子,如何利用构效关系,以结构生物学为基础,快速合成众多新分子成为研。
21、随着药物研发全球化进程的发展,作为具有大量人口资源疾病种类分布广泛研究费用相对较低的发展中国家,中国必然成为跨国公司进行国际多中心临床试验的重要选择地点,另一方面,该试验也是后续申请受试药物进口中国必要的铺垫。 2007 年药品注册管理办法局。
22、 国家药品监督管理局 2021 年 12 月 目目 录录 一背景 . 1 二罕见疾病药物研发的特殊考虑 . 2 1获取罕见疾病临床数据 . 2 2关注生物标志物的应用 . 3 3积极应用定量药理学工具 . 4 4鼓励建立患者登记系统 . 4。
23、 1 敬请参阅最后一页特别声明 市场价格 人民币 : 76.00 元 目标价格 人民币 :81.92 元 市场数据市场数据人民币人民币 总股本亿股 9.11 已上市流通 A股亿股 4.28 流通港股亿股 2.19 总市值亿元 692.18 。
24、 1 敬请参阅最后一页特别声明 市场价格 人民币 : 84.03 元 目标价格 人民币 :99.88 元 市场数据市场数据 人民币人民币 总股本亿股 1.08 已上市流通 A股亿股 0.25 总市值亿元 90.89 年内股价最高最低元 10。
25、请务必阅读正文之后的重要声明部分请务必阅读正文之后的重要声明部分 评级评级:买入买入首次覆盖首次覆盖 市场价格:市场价格:2 26.906.90 元元 股股 分析师:闻学臣分析师:闻学臣 执业证书编号:执业证书编号:S07405190900。
26、最后,加强临床试验的多样化参与,还可以提供可能挽救生命的疗法和高质量的保健服务,从而有助于改善卫生公平。 临床试验是患者接受未经批准的临床研究药物的主要途径。
27、 请务必阅读正文之后的信息披露和法律声明 TableMain 证券研究报告 公司首次覆盖 百诚医药301096.SZ 2022 年 04 月 15 日 买入买入首次首次 所属行业:医药生物 当前价格元:75.80 证券分析师证券分析师 陈铁。
【临床CRO】相关PDF文档

生物医药行业创新药研究框架之CSCO+ESMO2021分析:临床研发热点、国产药物临床数据及竞争格局解读-20211015(26页).pdf
上传时间: 2021-10-18 大小: 1.95MB 页数: 26
![【研报】医药生物行业CRO、CMO 系列报告(二):从IND和新开临床前瞻中国CRO行业发展前景-20200529[18页].pdf](/images/filetype/d_pdf.png)
【研报】医药生物行业CRO、CMO 系列报告(二):从IND和新开临床前瞻中国CRO行业发展前景-20200529[18页].pdf
上传时间: 2020-07-31 大小: 1.84MB 页数: 18
![【研报】医药生物行业CRO、CMO 系列报告(一):全球CRO行业趋于成熟在生物科技浪潮中焕发生机-20200309[23页].pdf](/images/filetype/d_pdf.png)
【研报】医药生物行业CRO、CMO 系列报告(一):全球CRO行业趋于成熟在生物科技浪潮中焕发生机-20200309[23页].pdf
上传时间: 2020-07-31 大小: 2.14MB 页数: 23
![【研报】医药行业CRO&CDMO投研体系之行业深度报告(系列一):国内CRO&CDMO行业高景气背景下的追赶与跨越-20200114[49页].pdf](/images/filetype/d_pdf.png)
【研报】医药行业CRO&CDMO投研体系之行业深度报告(系列一):国内CRO&CDMO行业高景气背景下的追赶与跨越-20200114[49页].pdf
上传时间: 2020-07-31 大小: 1.28MB 页数: 49
【临床CRO】相关资讯

 临床研究中数字端点有什么意义?数字健康技术有什么作用?
临床研究中数字端点有什么意义?数字健康技术有什么作用?
发布时间: 2023-04-27

 CRO公司是干什么的?商业模式有哪些?国内十大cro公司一览表
CRO公司是干什么的?商业模式有哪些?国内十大cro公司一览表
发布时间: 2023-04-27
 什么是肝素类药物?有哪些种类?肝素类药物的临床应用一览
什么是肝素类药物?有哪些种类?肝素类药物的临床应用一览
发布时间: 2023-04-27

 什么是紫杉醇类药物?有哪些?紫杉醇类药物的临床应用一览
什么是紫杉醇类药物?有哪些?紫杉醇类药物的临床应用一览
发布时间: 2022-04-19

 1300万一针“史上最贵药”获批临床,是什么药?为什么这么贵?
1300万一针“史上最贵药”获批临床,是什么药?为什么这么贵?
发布时间: 2022-01-20

 基因芯片在临床检测中的应用,与传统产前筛查优缺点分析
基因芯片在临床检测中的应用,与传统产前筛查优缺点分析
发布时间: 2021-07-21

 ICON:怎样提高临床试验研究的效率、有效性和质量?
ICON:怎样提高临床试验研究的效率、有效性和质量?
发布时间: 2021-07-16

 患者中心性在临床研究中的表现:以病人为中心的含义是什么?
患者中心性在临床研究中的表现:以病人为中心的含义是什么?
发布时间: 2021-04-21
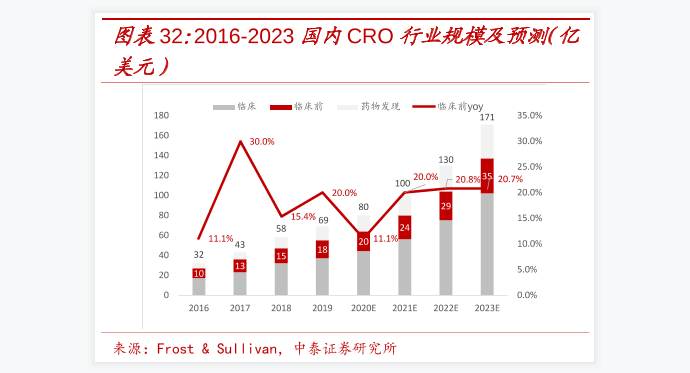
 2016-2023国内CRO行业规模及预测:预计2023年国内CRO行业最高规模达171亿元
2016-2023国内CRO行业规模及预测:预计2023年国内CRO行业最高规模达171亿元
发布时间: 2021-04-13

 艾滋病治疗发展现状和前景报告:临床试验采用数字健康技术
艾滋病治疗发展现状和前景报告:临床试验采用数字健康技术
发布时间: 2021-03-25

 精准医学护理可获得性和临床实用性研究模型分析
精准医学护理可获得性和临床实用性研究模型分析
发布时间: 2021-02-24

 亿欧智库:费森尤斯卡比中国临床营养业务研究报告:临床营养巨头企业如何面对特医食品新浪潮?(附下载)
亿欧智库:费森尤斯卡比中国临床营养业务研究报告:临床营养巨头企业如何面对特医食品新浪潮?(附下载)
发布时间: 2020-12-10
【临床CRO】相关词条

 CRO(合同研究组织)
CRO(合同研究组织)
发布时间: 2022-08-20
【临床CRO】相关数据

 预计2023年中国CRO市场规模约为214亿美元(附原数据表)
预计2023年中国CRO市场规模约为214亿美元(附原数据表)
发布时间: 2022-04-18

 中国CRO行业市场规模大不大?(附原数据表)
中国CRO行业市场规模大不大?(附原数据表)
发布时间: 2021-12-21

 2021年CRO/CDMO市场规模达到多少?
2021年CRO/CDMO市场规模达到多少?
发布时间: 2021-10-22


 最新报告
最新报告

 中英对照
中英对照
 全文搜索
全文搜索
 报告精选
报告精选
 PDF上传翻译
PDF上传翻译
 多格式文档互转
多格式文档互转
 入驻&报告售卖
入驻&报告售卖
 会员权益
会员权益

 机构报告
机构报告

 券商研报
券商研报
 财报库
财报库
 专题合集
专题合集
 英文报告
英文报告
 数据图表
数据图表
 会议报告
会议报告
 其他资源
其他资源





 新质生产力
新质生产力
 DeepSeek
DeepSeek
 低空经济
低空经济
 大模型
大模型
 AI Agent
AI Agent
 AI Infra
AI Infra
 具身智能
具身智能
 自动驾驶
自动驾驶
 宠物
宠物
 银发经济
银发经济
 人形机器人
人形机器人
 企业出海
企业出海
 算力
算力
 微短剧
微短剧
 薪酬
薪酬
 白皮书
白皮书
 创新药
创新药

 行业分析
行业分析
 个股研究
个股研究
 年报财报
年报财报
 IPO招股书
IPO招股书
 会议纪要
会议纪要
 宏观策略
宏观策略
 政策法规
政策法规
 其他
其他
 人工智能
人工智能
 信息科技
信息科技
 互联网
互联网
 消费经济
消费经济
 汽车交通
汽车交通
 电商零售
电商零售
 传媒娱乐
传媒娱乐
 医疗健康
医疗健康
 投资金融
投资金融
 能源环境
能源环境
 地产建筑
地产建筑
 传统产业
传统产业
 英文报告
英文报告
 其它
其它
 行业聚焦
行业聚焦
 芯片产业
芯片产业
 热点概念
热点概念
 全球咨询智库
全球咨询智库
 人工智能
人工智能
 500强
500强
 新质生产力
新质生产力
 会议峰会
会议峰会
 新能源汽车
新能源汽车
 企业年报
企业年报
 互联网
互联网
 公司研究
公司研究
 行业综观
行业综观
 消费教育
消费教育
 科技通信
科技通信
 医药健康
医药健康
 人力资源
人力资源
 投资金融
投资金融
 汽车产业
汽车产业
 物流地产
物流地产
 电子商务
电子商务
 传统产业
传统产业
 传媒营销
传媒营销
 其它
其它

 2025年养老经济/银发经济/长寿经济/银发族/老龄化报告合集(共50套打包)
2025年养老经济/银发经济/长寿经济/银发族/老龄化报告合集(共50套打包)


 2025年商业航天行业报告合集(共41套打包)
2025年商业航天行业报告合集(共41套打包)



 AI、科技与通信
AI、科技与通信
 广告、传媒与营销
广告、传媒与营销
 消费、零售与支付
消费、零售与支付
 HR、文化与旅游
HR、文化与旅游
 金融、保险与投资
金融、保险与投资
 能源、环境与工业
能源、环境与工业
 医疗制药与大健康
医疗制药与大健康
 物流、地产与建筑
物流、地产与建筑
 其他行业
其他行业












 AI ▪ 科技 ▪ 通信
AI ▪ 科技 ▪ 通信
 数字化
数字化
 金融财经
金融财经
 智能制造
智能制造
 电商传媒
电商传媒
 地产建筑
地产建筑
 医疗医学
医疗医学
 能源化工
能源化工
 其他行业
其他行业

 收藏
收藏 下载
下载 2025-11-19
2025-11-19

 AI查数
AI查数

 行业数据
行业数据
 政策法规
政策法规
 商业模式
商业模式
 产业链
产业链
 竞争格局
竞争格局
 市场规模
市场规模
 产业概述
产业概述
 其它
其它
 2025年
2025年 AI读财报
AI读财报

 年报
年报
 一季报
一季报
 半年报
半年报
 三季报
三季报
 IPO招股书
IPO招股书
 社会责任报告
社会责任报告
 A股
A股
 IPO申报
IPO申报
 港股
港股
 美股&全球
美股&全球
 新三板
新三板











 0731-84720580
0731-84720580
 商务合作:really158d
商务合作:really158d


 友链申请 (QQ):1737380874
友链申请 (QQ):1737380874





 微信扫码登录
微信扫码登录






 手机快捷登录
手机快捷登录

 账号登录
账号登录

