1、生物类似药
生物类似药中文通常称为生物相似药、生物相似物、生物仿制药,英文名称包括 biosimilars、similar biologics、Follow-on
biologics等,是指与原研生物药“高度相似”的生物药,其非活性成分与参照药可能有微小的差异,但在安全性、纯度和效能上并无实质差异。目前各个国家对生物仿制药的定义并不一样:
EMA将其定义为:是指与现存的生物药相似的生物药;
美国FDA定义为:是指与参照药高度相似的产品,它们在安全性、纯度和有效性没有临床意义上的差异;
WHO将其定义为:是指与已批准的生物治疗药物在质量、安全性和有效性上相似的生物治疗药物;
印度DBT将其定义为:与已批准的生物治疗药物在质量、安全性和有效性上相似的生物治疗药物;
加拿大卫生部将其定义为:通过展示与一个参照药相似,跟随一个在加拿大通过审批的版本上市的生物药;
韩国食品药品管理局将其定义为:与已批准的生物药物在质量、安全性和有效性上相似的生物药物;
日本卫生劳动与福利部将其定义为:与现存的生物药相似的生物药;
中国CFDA:在质量、安全性和有效性方面与已获准注册的参照药具有相似性的治疗用生物制品。
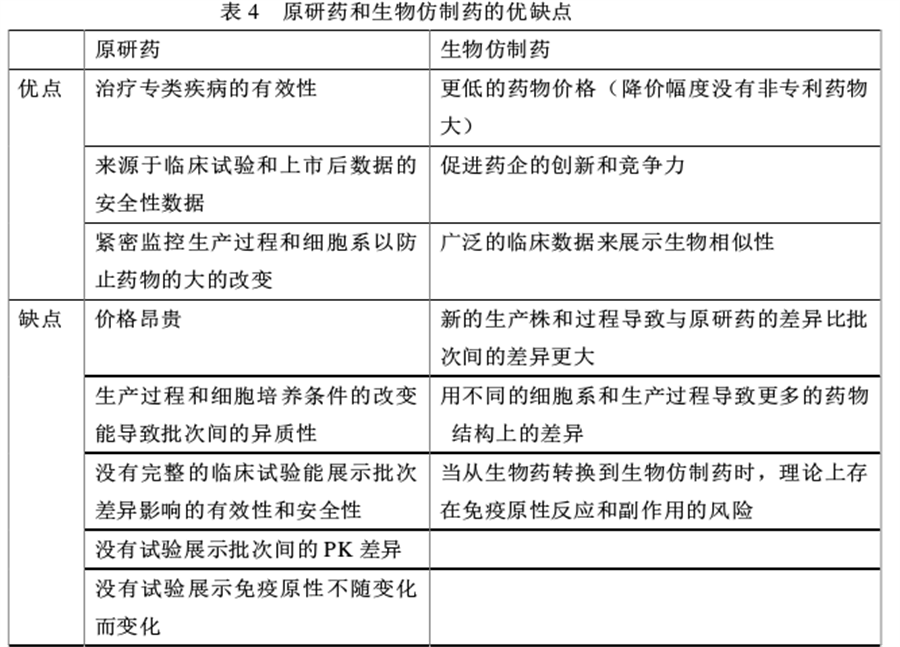
2、原研药和生物仿制药的优缺点
原研药
优点:
治疗专类疾病的有效性;来源于临床试验和上市后数据的安全性数据;紧密监控生产过程和细胞系以防止药物的大的改变。
缺点:
价格昂贵;生产过程和细胞培养条件的改变能导致批次间的异质性;没有完整的临床试验能展示批次差异影响的有效性和安全性;没有试验展示批次间的PK差异;没有试验展示免疫原性不随变化而变化。
生物类似药
优点:
更低的药物价格(降价幅度没有非专利药物大);促进药企的创新和竞争力;广泛的临床数据来展示生物相似性。
缺点:
新的生产株和过程导致与原研药的差异比批次间的差异更大;用不同的细胞系和生产过程导致更多的药物结构上的差异;当从生物药转换到生物仿制药时,理论上存在免疫原性反应和副作用的风险。
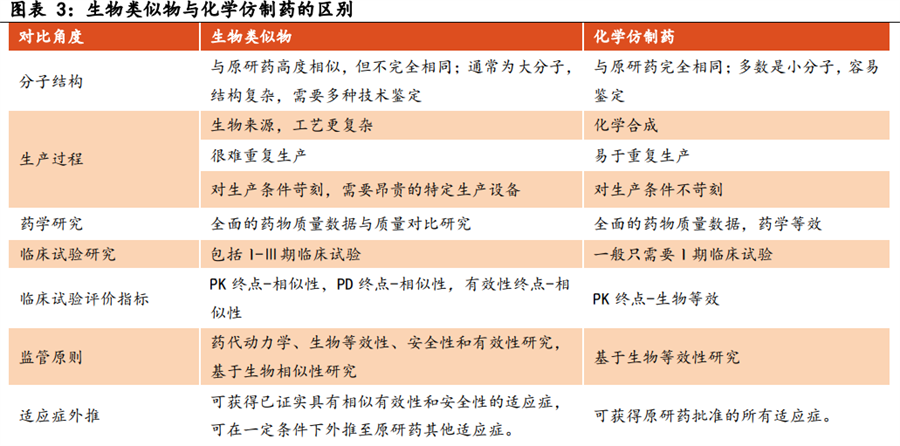
3、生物类似药与化学仿制药区别
(1)分子结构
生物类似药:与原研药高度相似,但不完全相同;通常为大分子,结构复杂,需要多种技术鉴定
化学仿制药:与原研药完全相同;多数是小分子,容易鉴定
(2)生产过程
生物类似药:生物来源,工艺更复杂;很难重复生产;对生产条件苛刻,需要昂贵的特定生产设备
化学仿制药:化学合成;易于重复生产;对生产条件不苛刻
(3)药学研究
生物类似药:全面的药物质量数据与质量对比研究
化学仿制药:全面的药物质量数据,药学等效
(4)临床试验研究
生物类似药:包括I-Ⅲ期临床试验
化学仿制药:一般只需要I期临床试验
(5)临床试验评价指标
生物类似药:PK 终点-相似性,PD 终点-相似性,有效性终点-相似性
化学仿制药:PK 终点-生物等效
(6)监管原则
生物类似药:药代动力学、生物等效性、安全性和有效性研究,基于生物相似性研究
化学仿制药:基于生物等效性研究
(7)适应症外推
生物类似药:可获得已证实具有相似有效性和安全性的适应症,可在一定条件下外推至原研药其他适应症
化学仿制药:可获得原研药批准的所有适应症
推荐阅读:《沙利文咨询公司:中国生物类似药市场研究报告(上)[25页].pdf》
《【研报】医药生物行业科创板专题报告之六:百奥泰—聚焦生物类似物及创新药研发-20200219[17页].pdf》
《科睿唯安:2021未来仿制药竞争格局与机会(30页).pdf》

 0731-84720580
0731-84720580
 商务合作:really158d
商务合作:really158d


 友链申请 (QQ):1737380874
友链申请 (QQ):1737380874





 微信扫码登录
微信扫码登录





